CMTA (Charcot–Marie–Tooth Association) lider w dążeniu do zgłębienia możliwości terapii genowej w leczeniu CMT, już teraz wyobraża sobie możliwości, jakie terapia genowa stwarza dla naszej globalnej społeczności 2,8 miliona ludzi z CMT. CMTA poszerza program Strategii Przyspieszenia Badań (ang. Strategy to Accelerate Research; STAR) i Radę Doradczą STAR (ang. STAR Advisory Board).
W przypadku CMT przyczyny genetyczne wielu typów CMT są już znane, co pozwala naukowcom skuteczniej skoncentrować się na genetycznych rozwiązaniach leczenia – i prawdopodobnie wyleczenia – tej choroby. Kontynuując badania nad terapią genową w laboratorium, naszym ostatecznym celem jest przekształcenie ich w skuteczne metody leczenia osób żyjących z CMT.
Biorąc pod uwagę większą wykonalność i zastosowanie terapii genowej w CMT, w roku 2018 CMTA zorganizowało Warsztaty Terapii Genowej. W odpowiedzi na zaproszenia wystosowane przez członka zarządu CMTA, dr Stevena Scherera, ponad 20 czołowych ekspertów w dziedzinie terapii genowej zebrało się na inauguracyjnych warsztatach CMT, których przewodnim tematem była terapia genowa. W spotkaniu uczestniczyli eksperci, którzy pracowali w powiązanych obszarach chorób genetycznych, neurologicznych i mięśni, a także klinicyści i naukowcy inicjujący starania na rzecz terapii genowej CMT2D i CMT4J.
Na podstawie wniosków z tego spotkania, CMTA powiększyła Naukową Rade Doradczą o kilku ekspertów, aby sformułować strategie terapii genowej dla podtypów CMT2 i CMT1. Należą do nich dr med. Kleopas Kleopa z Cypryjskiego Instytutu Neurologii i Genetyki (ang. Cyprus Institute of Neurology & Genetics), dr Scott Harper ze Stanowego Uniwersytetu Medycznego Ohio (ang. Ohio State University School of Medicine) oraz dr Steven Gray z Południowo-Zachodniego Centrum Medycznego Uniwersytetu Teksańskiego (ang. University of Texas Southwestern Medical Center), z których każdy był inicjatorem projektów poświęconych terapiom genowym CMT. Dr Kleopa jest neurologiem nerwowo-mięśniowym, który udowodnił słuszność koncepcji, że terapia genowa działa w dwóch mysich modelach CMT: CMT1X i CMT4C. Kontynuuje również starania w celu opracowania nowatorskich terapii w CMT1A. Dr Harper pracował intensywnie nad dystrofią mięśniową i współpracuje z dr Robertem Burgessem w Laboratorium Jackson nad opracowaniem terapii genowej w CMT2D. Podstawową dziedziną specjalizacji dr Graya jest inżynieria wektorów terapii genowej wirusów związanych z adenowirusami (AAV), a następnie optymalizacja strategii dostarczania genu do układu nerwowego. Prowadzi on także prace nad opracowaniem nowatorskiej terapii genowej dla dwóch typów CMT: GAN i CMT4J.
Nasze geny dyktują wiele naszych cech osobistych; jednak mutacje w genach powodują choroby genetyczne, takie jak CMT. Naukowcy od dziesięcioleci pracują nad modyfikacją lub zastąpieniem wadliwych genów zdrowymi, aby leczyć choroby lub im zapobiegać. Na szczęście obserwujemy znaczny postęp w tych staraniach nad zapewnieniem opcji terapii genowej dla CMT. W rzeczywistości ostatnie badania zapewniły skuteczną terapię genową w rdzeniowym zaniku mięśni (SMA), wyniszczającej chorobie, która atakuje te same neurony ruchowe, na które wpływa CMT.
Czasami cały gen jest zduplikowany, jak w CMT1A, gdzie fragment chromosomu wokół genu PMP22 występuje w trzech kopiach zamiast w dwóch. Alternatywnie, część genu jest uszkodzona lub brakuje jej od urodzenia, co powoduje wiele innych znanych form CMT. Każda z tych zmian może zaburzyć strukturę białka kodowanego przez taki gen, powodując problemy na poziomie komórkowym, które ostatecznie prowadzą do choroby.
W terapii genowej naukowcy mogą zrobić jedną z kilku rzeczy w zależności od problemu z genem. Najprostszą formą terapii genowej jest po prostu dostarczenie prawidłowej kopii genu, co jest podstawą terapii genowej SMA. W różnych odmianach tego podejścia można stłumić geny powodujące problemy. Jednym z przykładów jest niedawne wykazanie, że oligonukleotydy antysensowne mogą być stosowane do poprawy neuropatii w modelach gryzoni CMT1A. Ponadto ekscytująca nowa dziedzina edycji genomu przy użyciu technologii CRISPR umożliwiła obecnie korygowanie mutacji powodujących choroby, a wspólne projekty zostały już zainicjowane z liderami w tej dziedzinie.
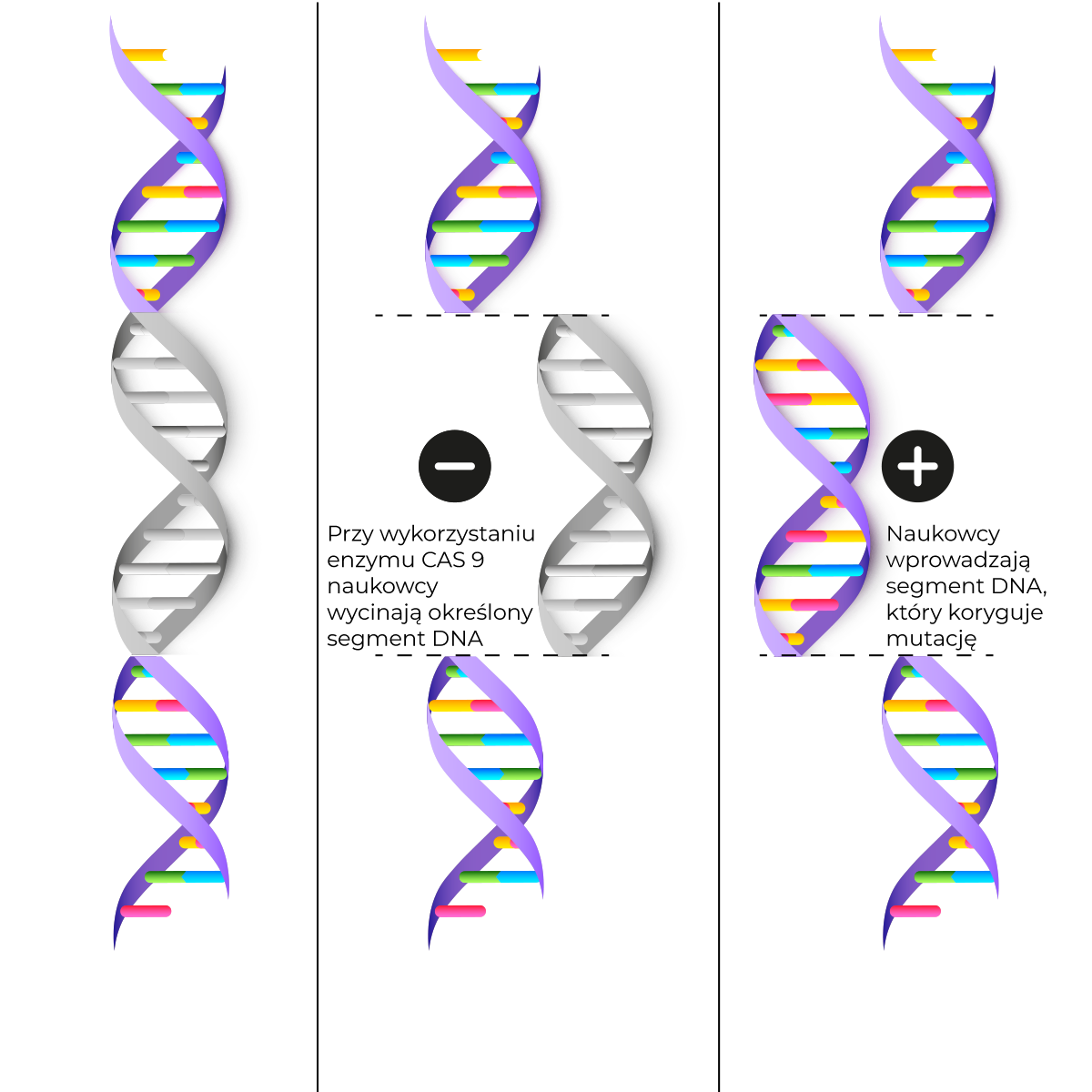
Aby wstawić nowe geny bezpośrednio do komórek, naukowcy używają nośnika zwanego wektorem, który jest genetycznie modyfikowany w celu dostarczenia prawidłowej wersji genu. Na przykład wirusy mają naturalną zdolność dostarczania materiału genetycznego do komórek, a zatem mogą być używane jako wektory. Podczas gdy niektóre wirusy powodują choroby, wektory wirusowe są wysoce zmodyfikowane w celu wyeliminowania ich zdolności do wywoływania choroby, tak aby można je było bezpiecznie wykorzystywać do przenoszenia genów terapeutycznych do komórek ludzkich.
Terapia genowa może być stosowana do modyfikacji komórek wewnątrz lub na zewnątrz ciała. Kiedy robi się to wewnątrz ciała, lekarz wstrzykuje wektor niosący gen bezpośrednio do części ciała, w której znajdują się uszkodzone komórki.
Zanim firma będzie mogła wprowadzić na rynek produkt terapii genowej do stosowania u ludzi, produkt ten musi zostać przetestowany pod kątem bezpieczeństwa i skuteczności, aby amerykańska Agencja ds. Żywności i Leków (ang. Food and Drug Administration; FDA) mogła ocenić, czy ryzyko terapii jest dopuszczalne w świetle jej ewentualnych korzyści z jej stosowania. Terapie genowe zaczęły uzyskiwać aprobatę FDA, a wiele z nich jest w trakcie badań klinicznych.
W CMTA wierzymy, że terapia genowa daje obietnicę zapewnienia skutecznych terapii dla osób żyjących z CMT. Ponieważ ciągle robimy wielkie postępy w tej dziedzinie, CMTA angażuje się w przyspieszenie rozwoju strategii terapii genowej, inwestując w najbardziej obiecujące i przełomowe terapie genowe, które mogą przynieść korzyści naszej społeczności.